Laboratorní vyšetření v hepatologii je soubor biochemických vyšetření, která mohou odhalit poškození jater (funkční či morfologické) a současně posoudit závažnost tohoto poškození. Laboratorní vyšetření jsou ve většině doplněna zobrazovací metodou, event. jaterní biopsií.
Používané laboratorní testy můžeme rozdělit do několika skupin:
- testy odrážející poškození hepatocytu (ALT, AST)
- testy odrážející poruchu na úrovni žlučovodů a kanalikulárního pólu jaterní buňky (ALP, GGT)
- testy měřící syntetickou činnost jater (albumin, prealbumin, cholinesteráza, protrombinový komplex / koagulační faktory)
- testy měřící kapacitu jater transportovat organické anionty a odstraňovat endogenní a exogenní látky z cirkulace (bilirubin, žlučové kyseliny)
- testy měřící schopnost a kapacitu jater metabolizovat endogenní a xenogenní látky (např. amoniak, CDT, lidocain, aminopyrin)
- vyšetření nespecifických protilátek v diagnostice jaterních onemocnění
- imunologická a sérologická diagnostika hepatitid
- biochemická vyšetření u vybraných jaterních chorob
Testy odrážející poškození hepatocytu
Alaninaminotransferáza (ALT) je cytoplazmatický enzym vysoce specifický pro jaterní buňku. V menší míře se nachází např. v myokardu nebo kosterním svalu. Při mírném poškození jaterní buňky se ALT dostává do krve ve zvýšené míře. Průkaz zvýšené katalytické koncentrace ALT v krevním séru je velmi specifickým ukazatelem poškození jaterní buňky. Fyziologická hodnota ALT v krevním séru dospělého jedince je kolem 0,1–0,78 µkat/l.
Aspartátaminotransferáza (AST) je lokalizovaná v cytoplazmě i v mitochondriích jaterních buněk (cytoplazmatická a mitochondriální izoforma). AST není specifická jen pro játra, vyskytuje se v celé řadě dalších tkání (ledviny, srdeční sval, kosterní sval, mozek, slinivka břišní, červené krvinky). Cytoplazmatický izoenzym AST se dostává do krve, stejně jako ALT, i při jen lehkém postižení jaterních buněk. Mitochondriální izoenzym AST se uvolňuje do krve až při nekróze jaterních buněk. Fyziologická hodnota AST v krevní séru dospělého jedince je asi 0,05–0,72 µkat/l. Výraznější zvýšení sérové hodnoty AST je prognosticky závažnější než zvýšení ALT, protože signalizuje uvolnění cytoplazmatické i mitochondriální frakce
Testy odrážející poruchu na úrovni žlučovodů a kanalikulárního pólu jaterní buňky (ALP, GGT)
Alkalická fosfatáza (ALP) se nachází v několika izoformách (jaterní, kostní, střevní, placentární, …) ve všech buňkách lidského organismu. U zdravých jedinců je sérová koncentrace ALP podmíněna především její jaterní a kostní izoformou. Fyziologická hodnota koncentrace ALP v krevním séru dospělého jedince je asi 0,66–2,2 µkat/l.Zvýšené hodnoty doprovázejí především cholestázu (městnání žluči buď v játrech a/nebo mimojaterních žlučových cestách). Mezi další stavy zvyšující sérovou koncentraci ALP patří nemoci kostí (nádory včetně metastáz), nemoci jater včetně jejich metastatického postižení, revmatologické choroby či zvýšená funkce příštítných tělísek.
Gama-glutamyltransferáza (GGT) je enzym fyziologicky přítomný v membránách buněk s vysokou sekreční nebo absorpční aktivitou (játra, slinivka břišní, slezina, ledviny, prostata, srdce, mozek, placenta). V játrech se nachází v membráně jaterních buněk a v membráně buněk vystýlajících žlučové cesty (endotelové buňky žlučových cest). Fyziologická hodnota koncentrace GGT v krevním séru dospělého je asi 0,14–0,84 µkat/l. GGT se stanovuje většinou společně s ALP při podezření na onemocnění hepatobiliárního systému (jater a žlučových cest). Zvýšené sérové koncentrace nacházíme při městnání žluči v játrech, při akutních i chronických onemocnění jater včetně nádorů jater a při poškození jater dlouhodobým užíváním alkoholu. Hladina GGT však může stoupat i při některých mimojaterních onemocněních (infarkt myokardu, cukrovka, nádory slinivky břišní, chronická obstrukční bronchopulmonální nemoc apod.).
Testy měřící synteticku činnost jater (albumin, prealbumin, cholinesteráza, protrombinový komplex / koagulační faktory, plazmatické lipidy a lipoproteiny)
Albumin je syntetizován v játrech v denním množství 12–15 g. Stanovení koncentrace albuminu v krevním séru umožňuje odhadnout schopnost jater syntetizovat bílkoviny. Fyziologická koncentrace sérového albuminu je asi 35–53 g/l. Sérová hladina albuminu je ovlivňována jeho syntézou, distribucí a degradací, nutričním stavem, osmotickým tlakem i hormonálně (růstový hormon, kortikoidy, inzulin, glukagon, thyroxin). Dehydratovaní pacienti a pacienti léčeni diuretiky mohou mít hladinu albuminu zvýšenou. Snížená hodnota sérového albuminu může signalizovat jaterní onemocnění, onemocnění ledvin, popáleniny, protein-ztrácející enteropatii, malabsorpci, nedostatečný přísun bílkovin stravou, zánětlivé onemocnění aj.
Cholinesteráza je enzym vyskytující se v těle ve dvou formách – acetylcholinesteráza (též cholinesteráza I; vytváří se v synapsích cholinergních nervů a v nervosvalových ploténkách a je obsažena v erytrocytech) a selektivně hydrolyzuje acetylcholin, a příbuzný enzym (tzv. pseudocholinesteráza, choliesteráza II; vzniká v ribozomech jaterních buněk a je secernována do krve), který štěpí i jiné estery cholinu. V rámci diagnostiky onemocnění jater se používa stanovení druhého z uvedených enzymů, tj. pseudocholiesterázy / cholinesterázy II a oba výše uvedené enzymy tedy nelze zaměňovat. Nachází se v játrech, slinivce, srdci, séru a bílé hmotě mozkové. Snížení sérové aktivty značí snížení syntetické funcke jater a poukazuje na závažnou hepatopatii.
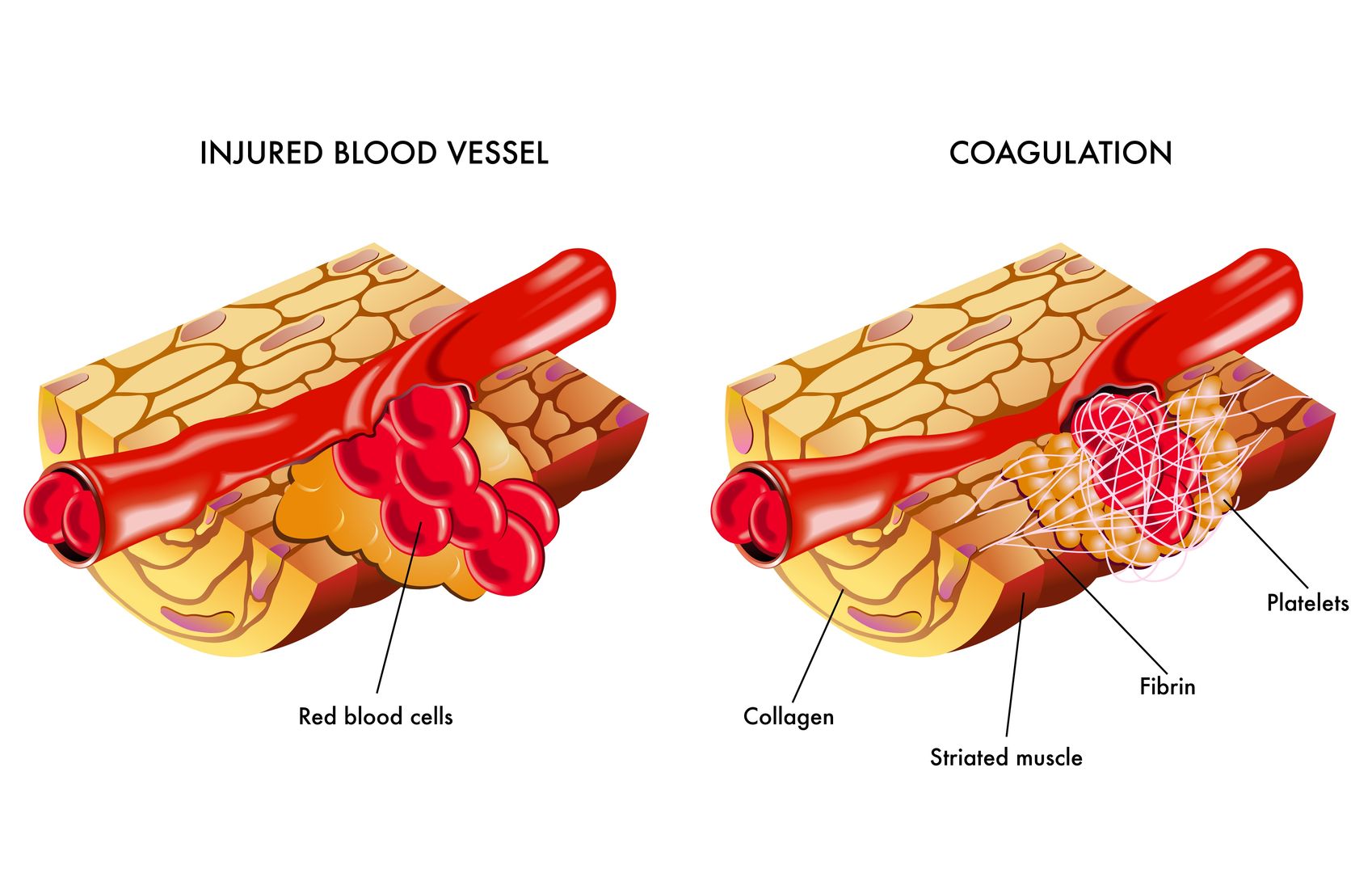
Koagulační faktory – v játrech je syntetizována řada koagulačních faktorů – fibrinogen, protrombin, faktory V, VII, IX a X. Většina těchto faktorů v séru je v nadbytku a pokles nastává až při významné poruše jaterní proteosyntetické funkce. Nejčastěji užíváme stanovení protrombinového času – tzv. Quickův test (hodnota INR), který zachycuje aktivitu zevního koagulačního systému. U akutních i chronických chorob může protrombinový čas sloužit jako prognostický ukazatel.
Plazmatické lipidy a lipoproteiny – játra jsou významným místem syntézy a metabolismu lipidů a lipoproteinů a jsou hlavním zdrojem plazmatických lipoproteinů. Při akutní jaterní lézi stoupají sérové koncentrace triglyceridů, klesají hodnoty esterů cholesterolu a vznikají abnormity v elektroforéze lipoproteinů, které jsou následkem jaterního deficitu lecitincholesterolacyltransferázy. U chronických jaterních poruch se setkáváme s obdobnými nálezy, změny však jsou méně výrazné. Hodnota cholesterolu je u nemocných většinou v normě a významně klesá až v pokročilé fázi jaterního selhávání. Vzestup koncentrace cholesterolu a fosfolipidů a někdy i triglyceridů provází cholestatická jaterní onemocnění.
Testy měřící kapacitu jater transportovat organické anionty a odstraňovat endogenní a exogenní látky z cirkulace (bilirubin, žlučové kyseliny)
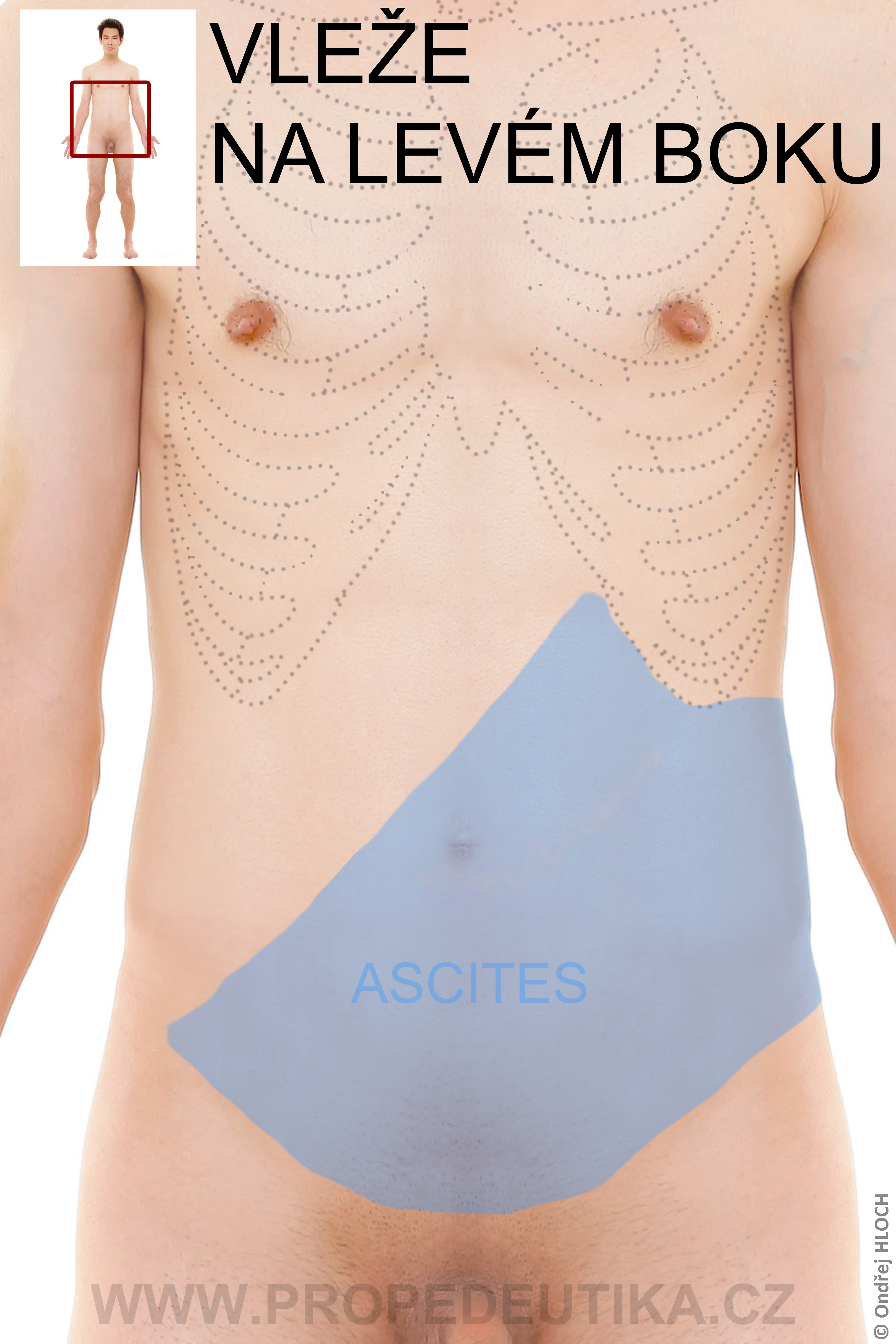
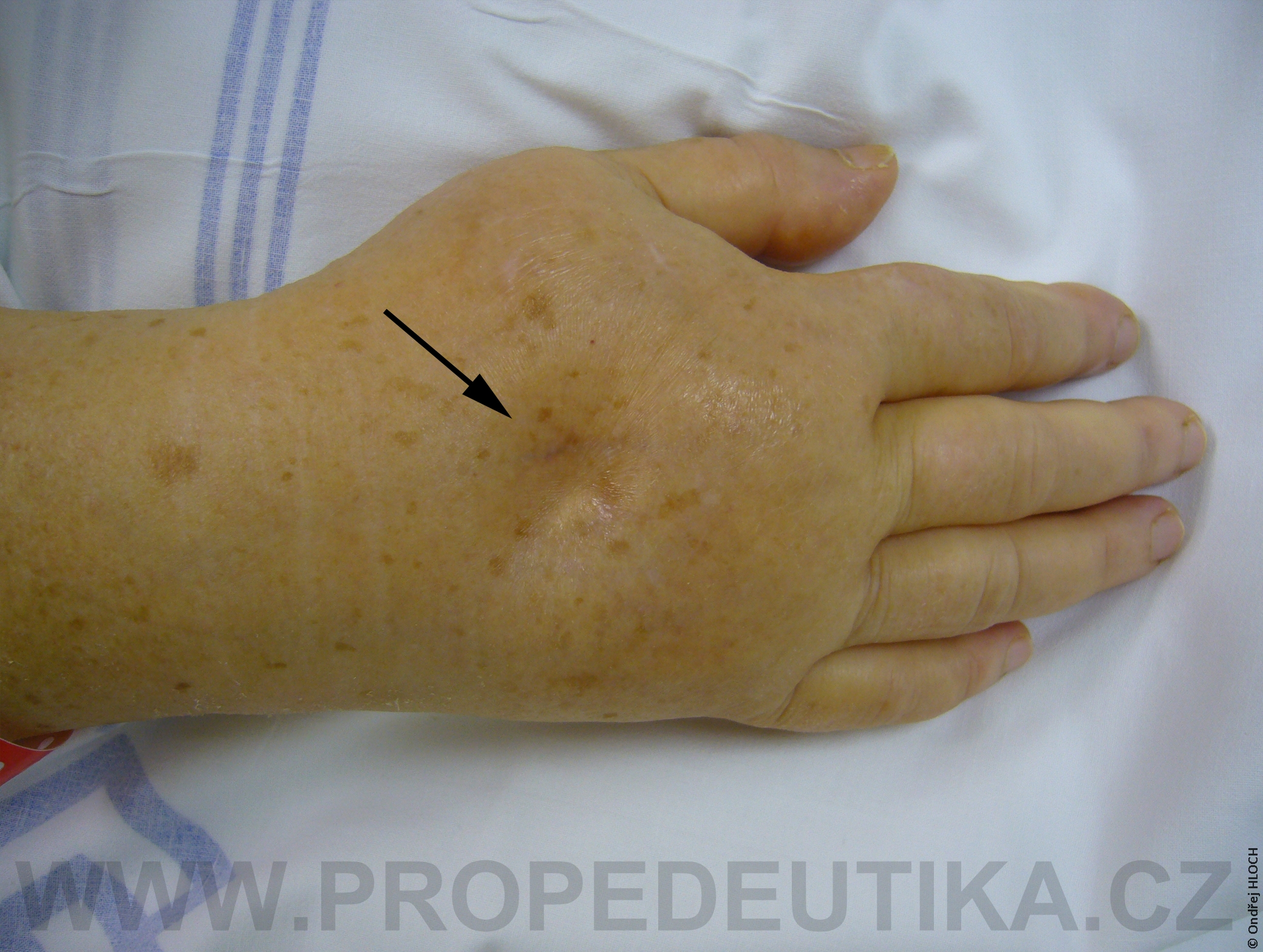
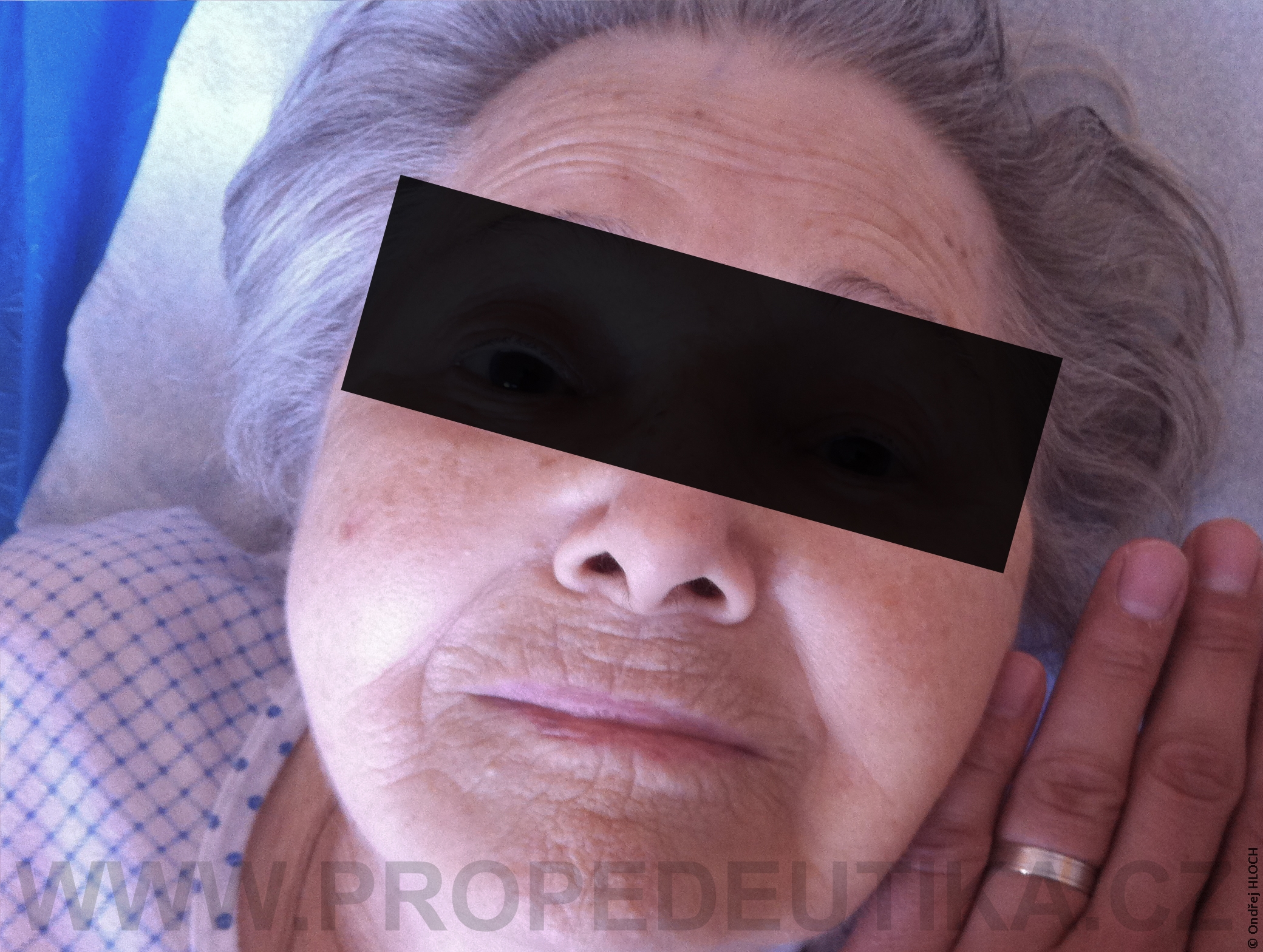
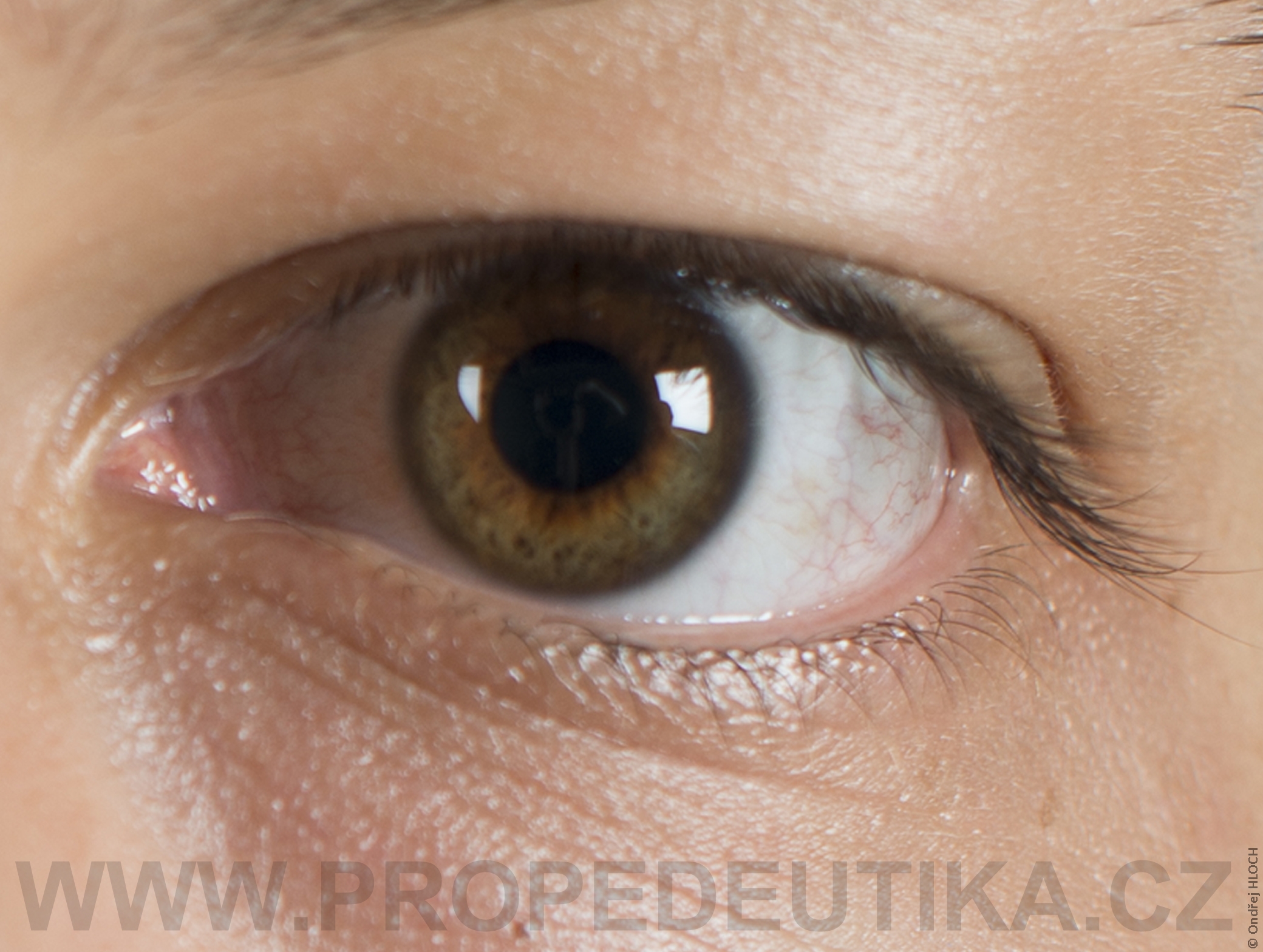
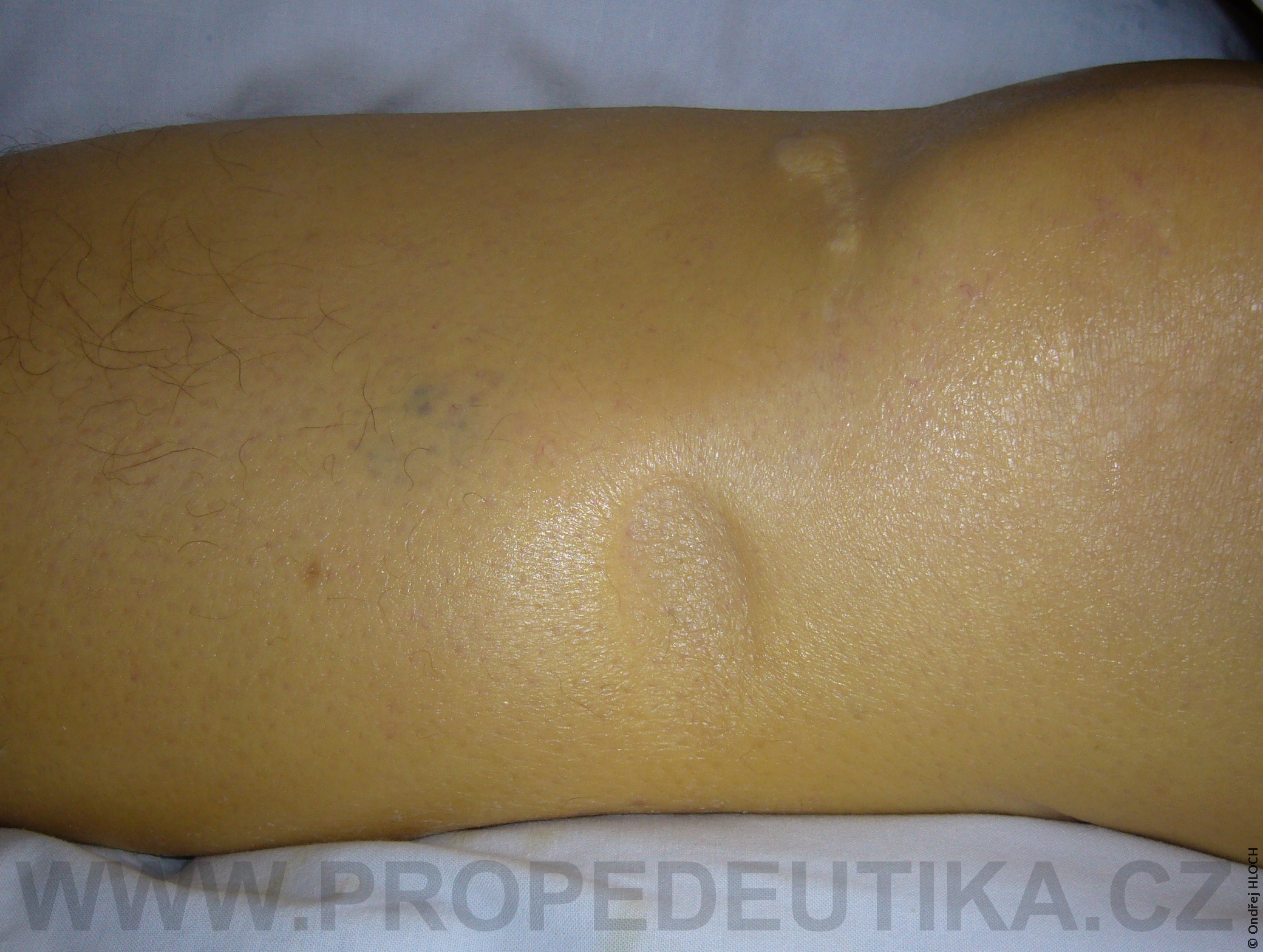
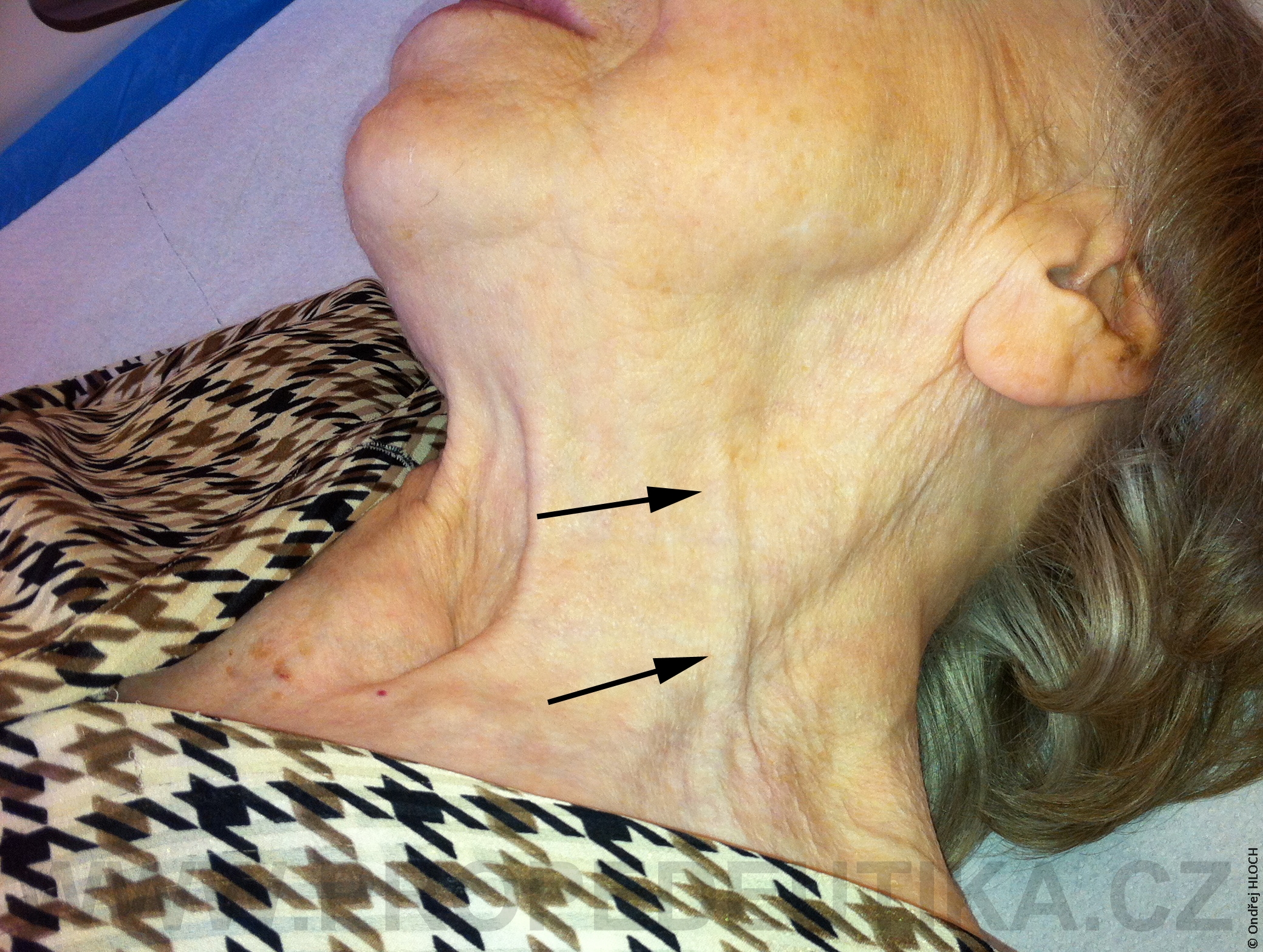
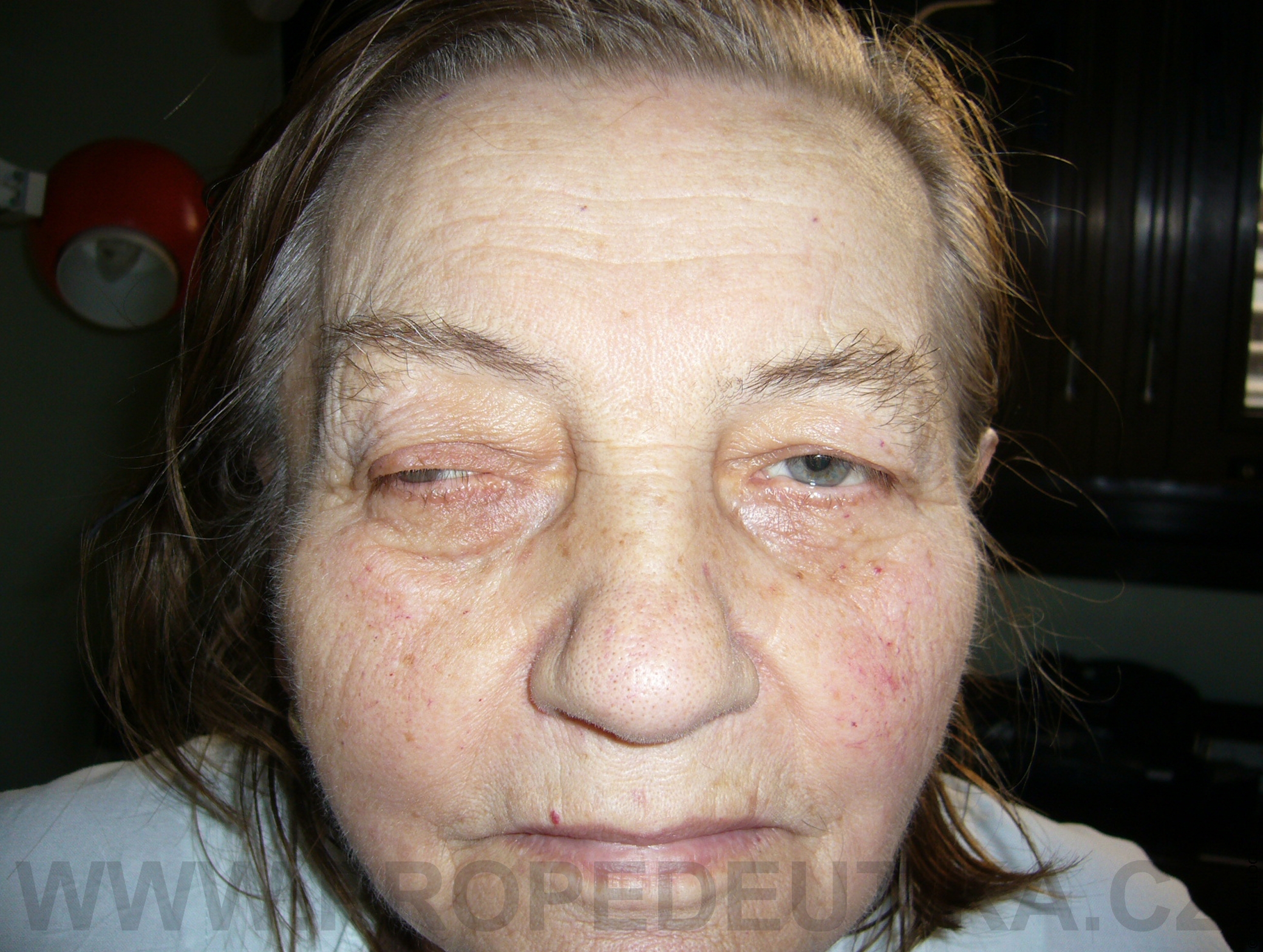
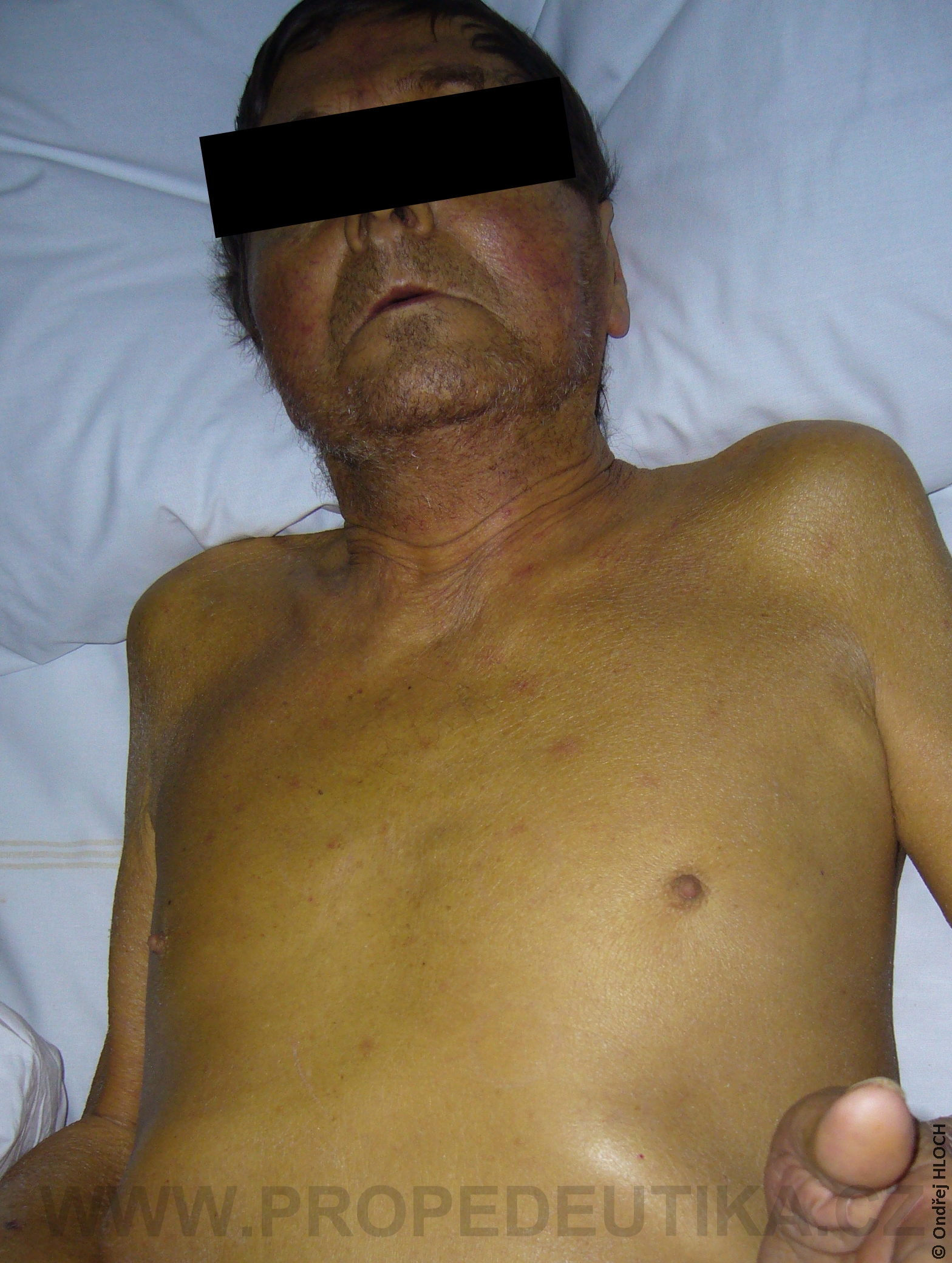
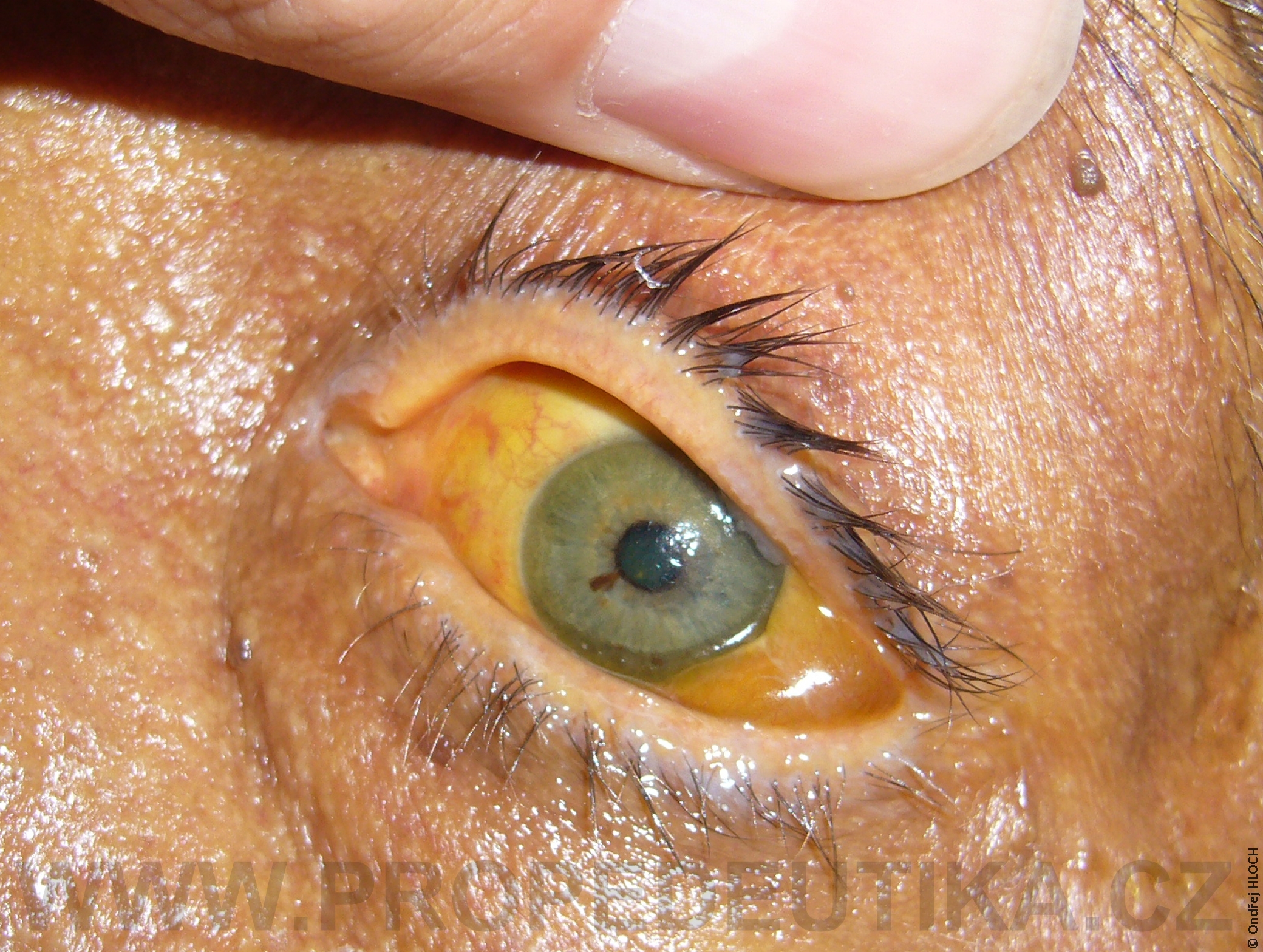
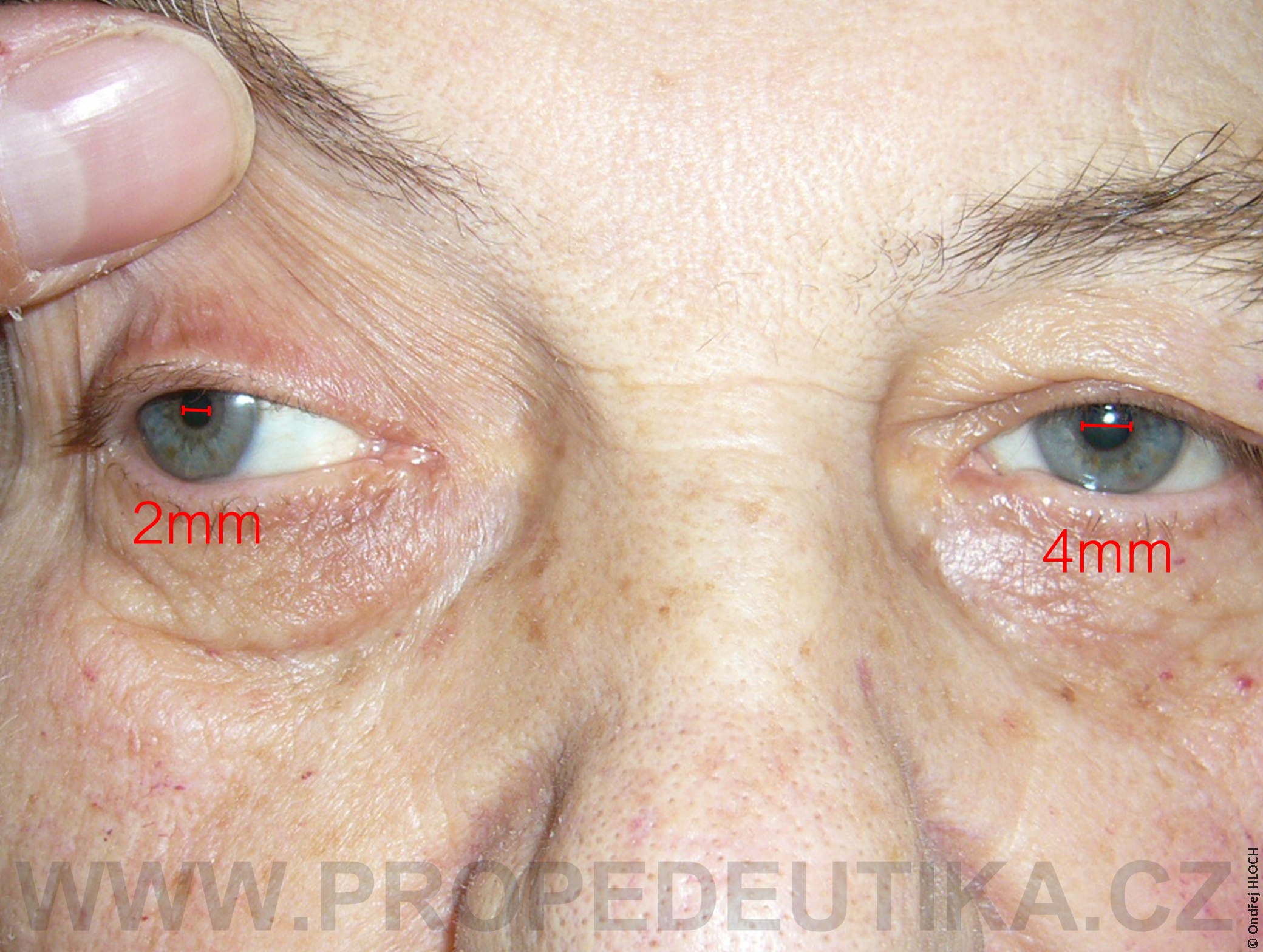
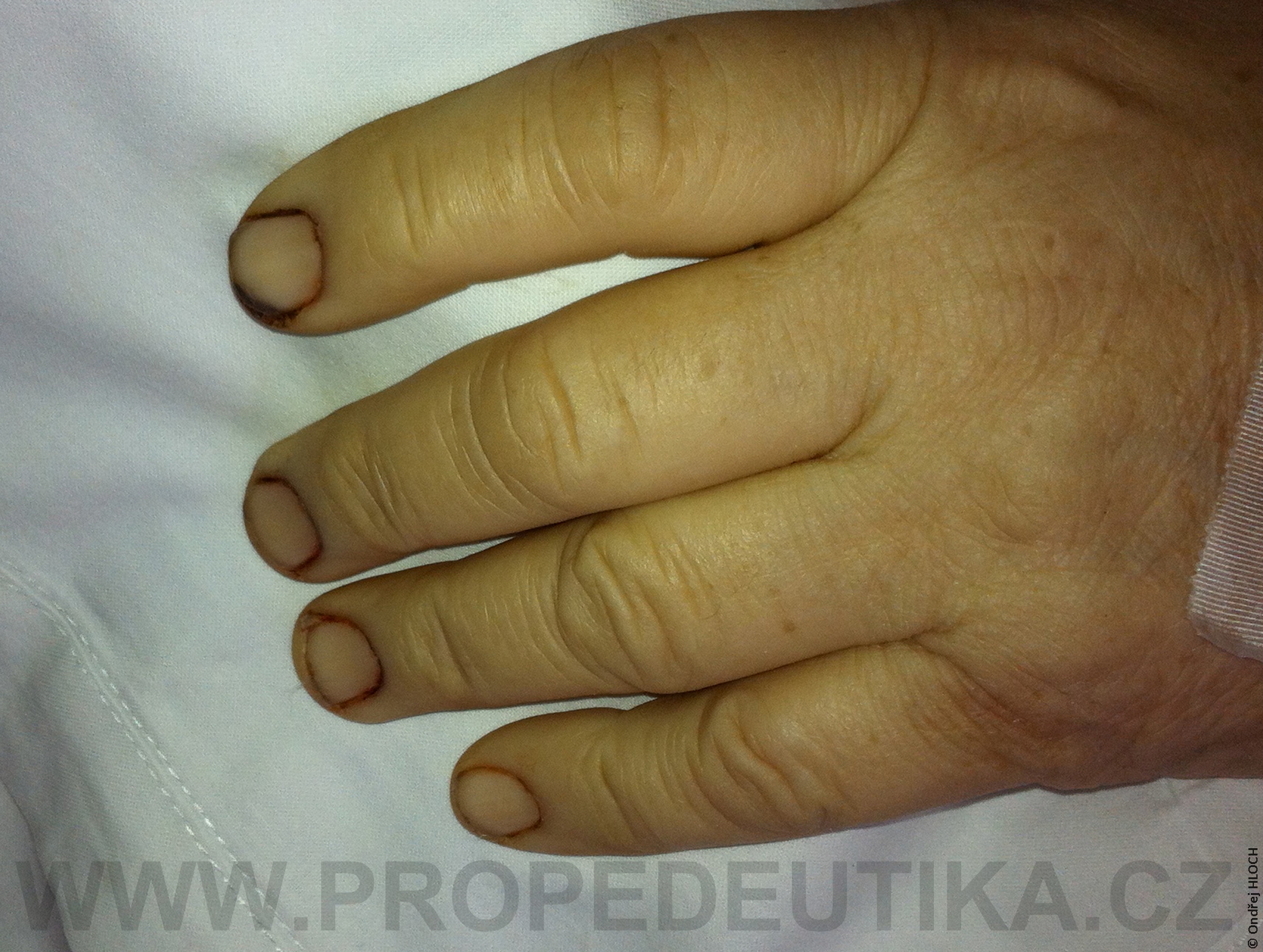
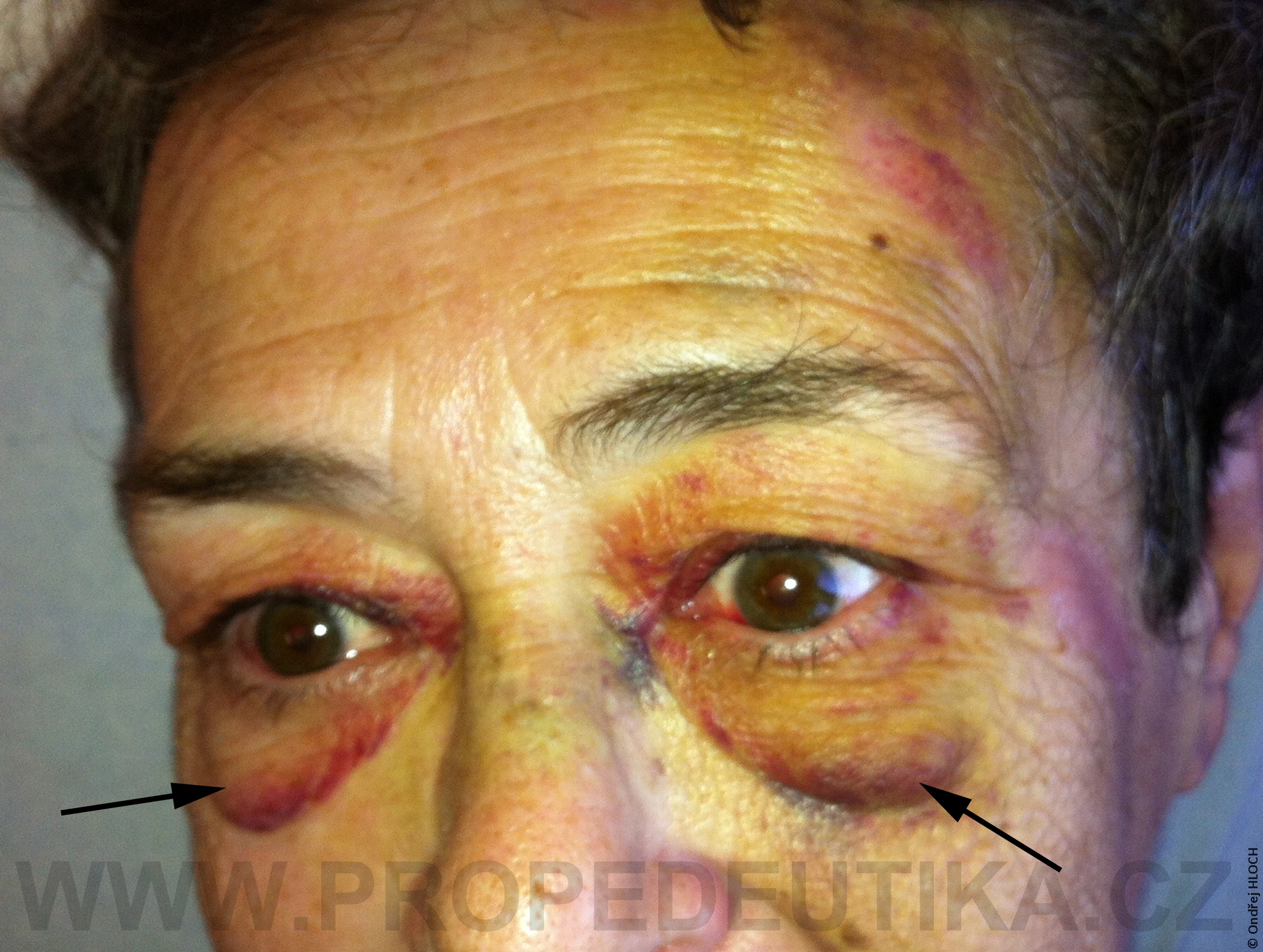
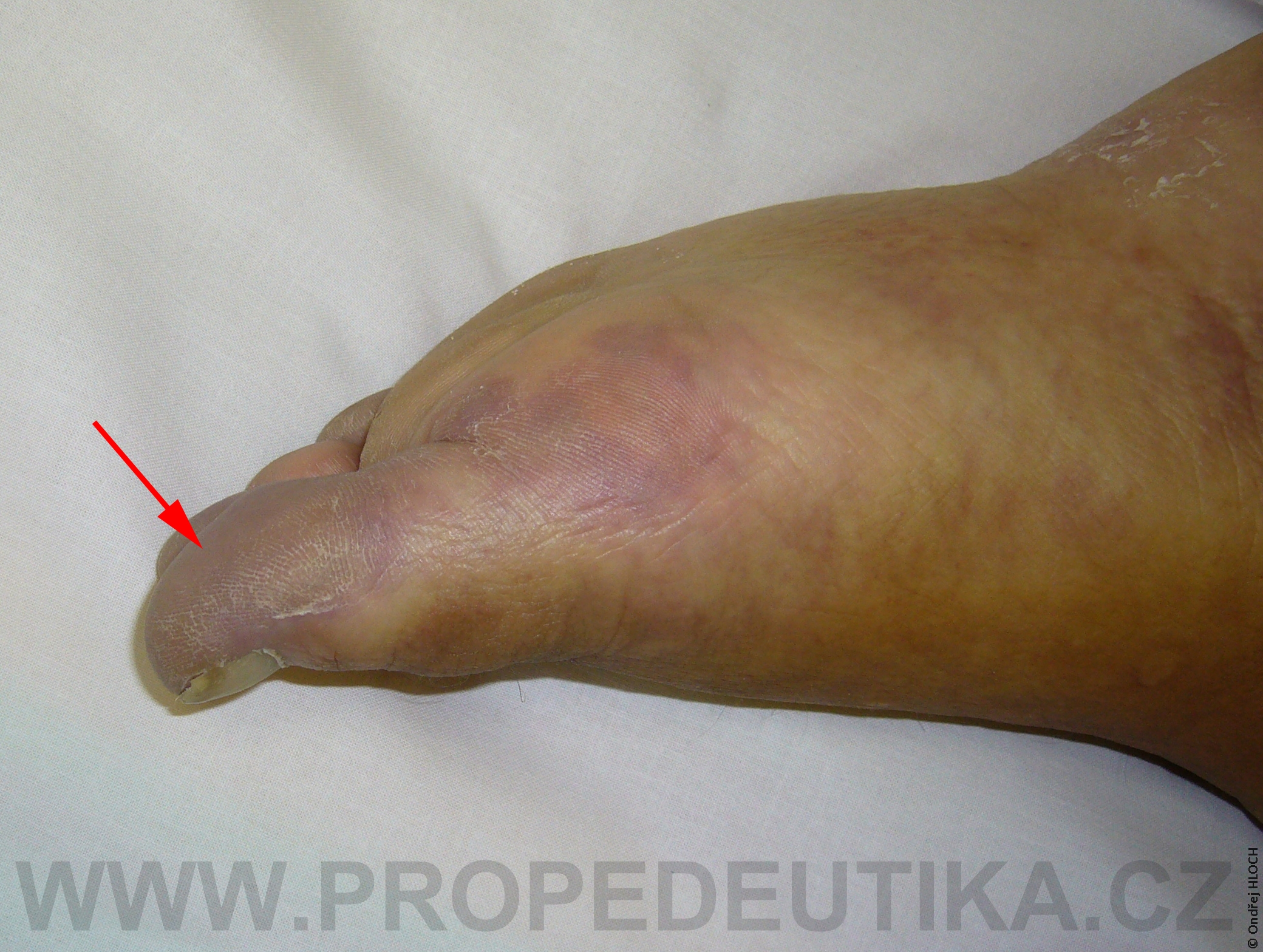
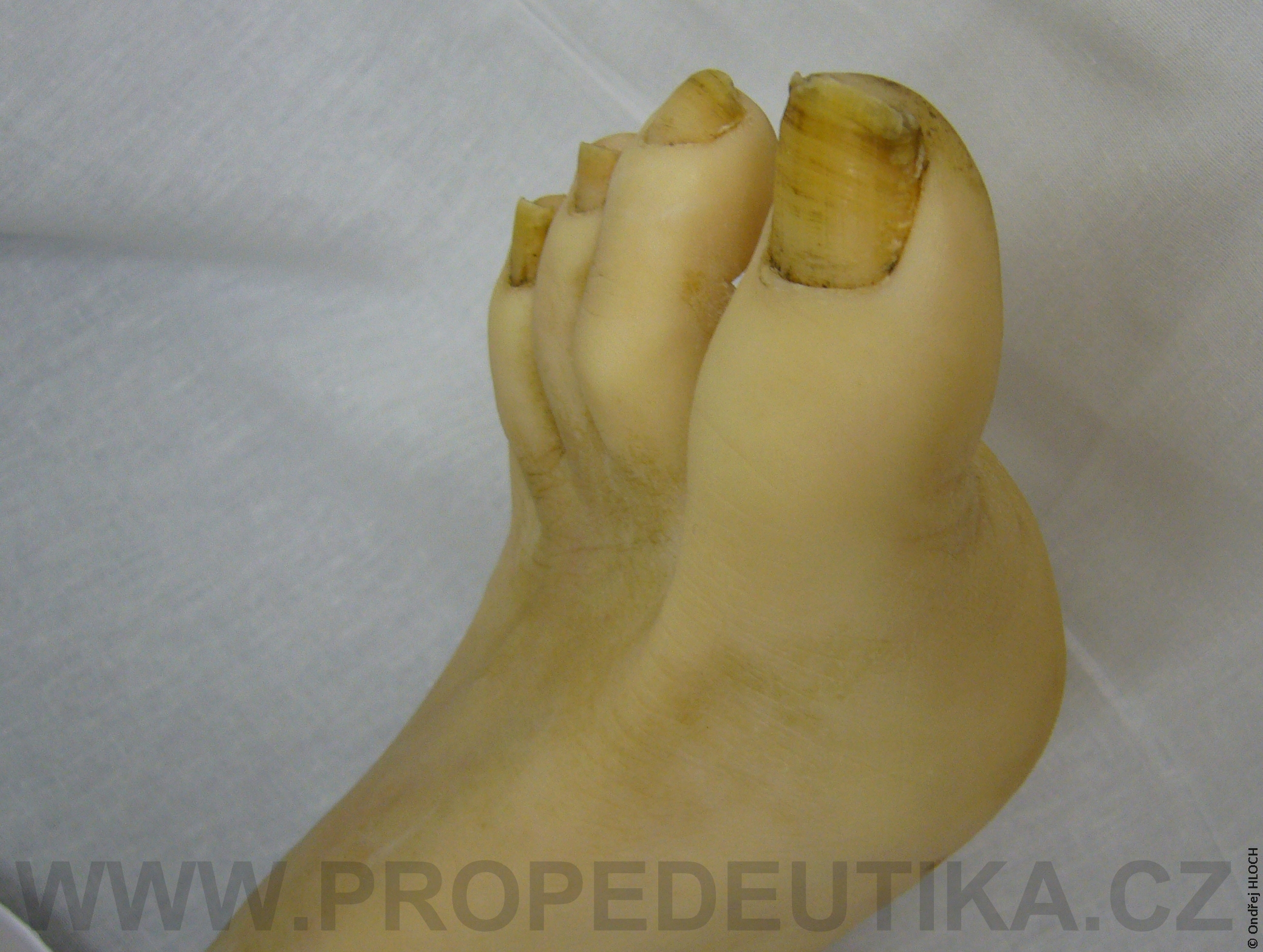
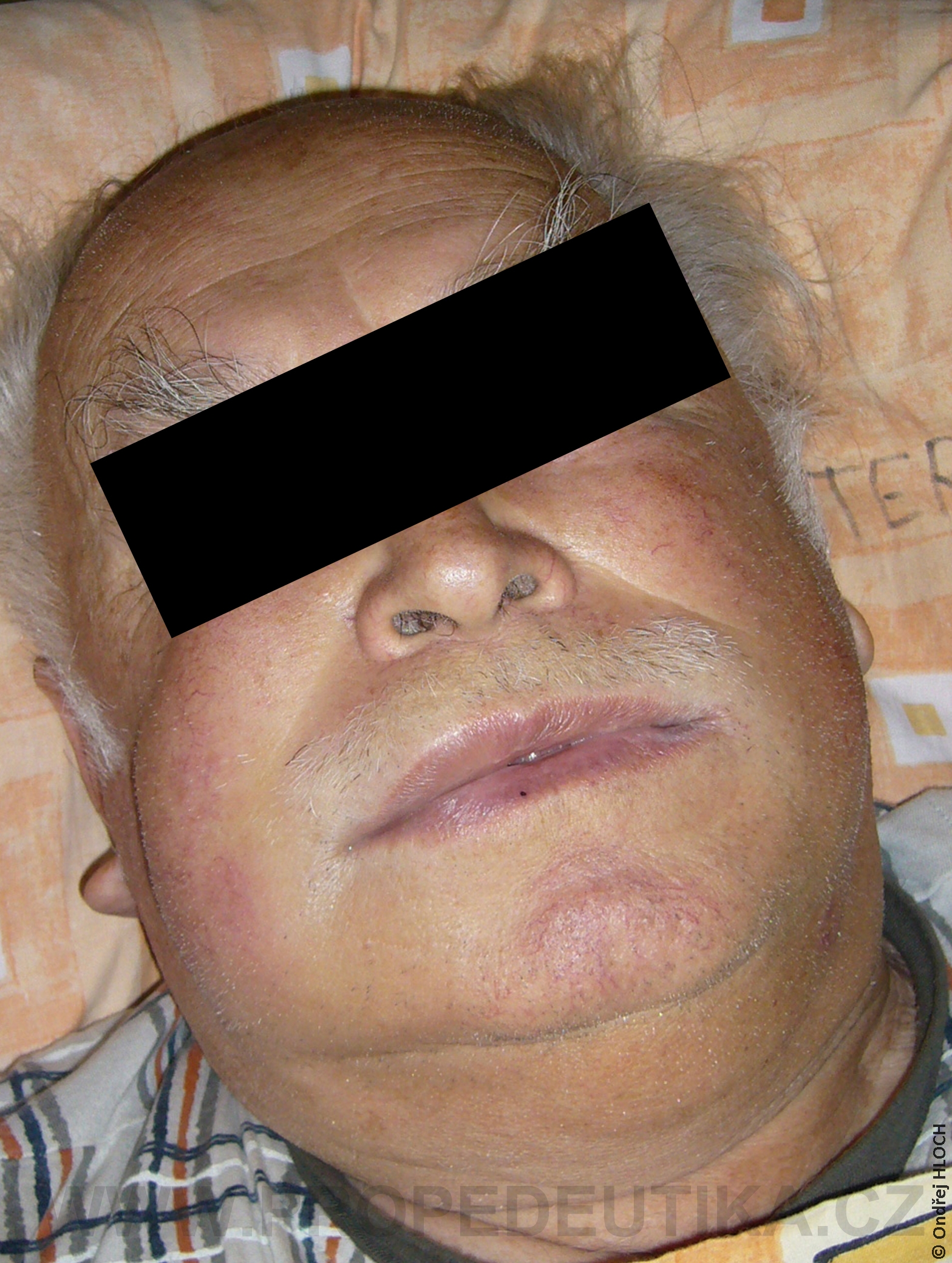
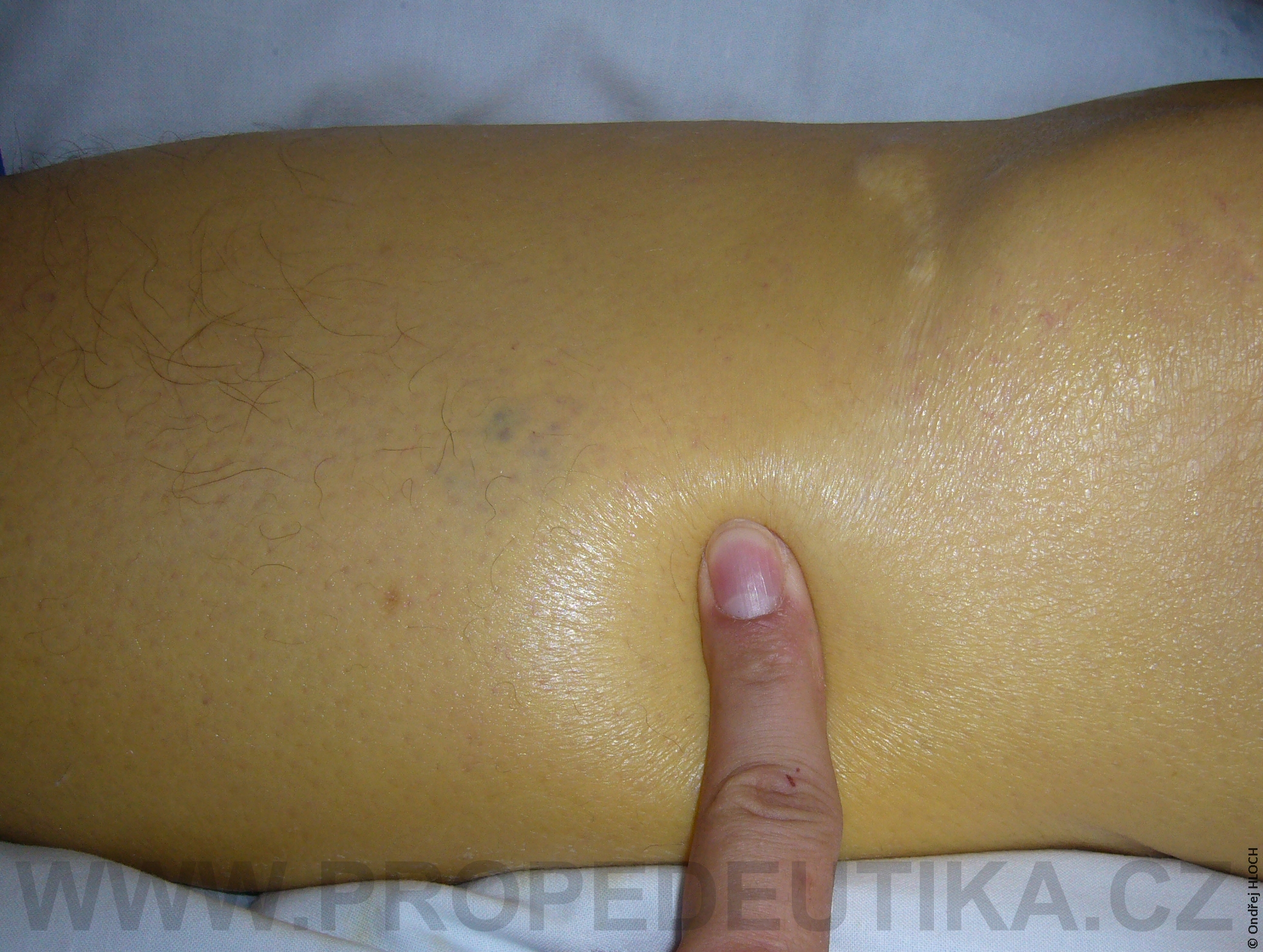
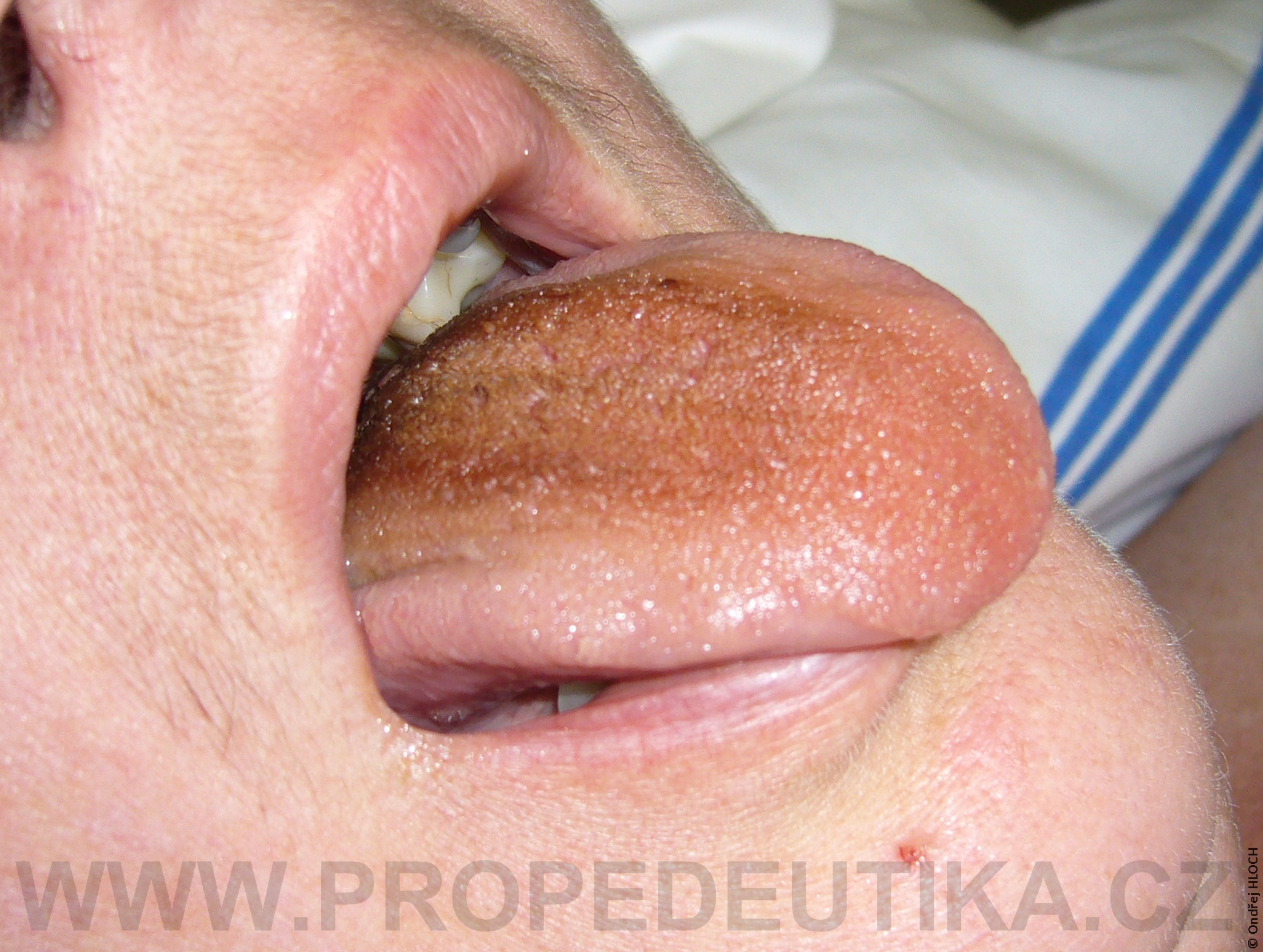
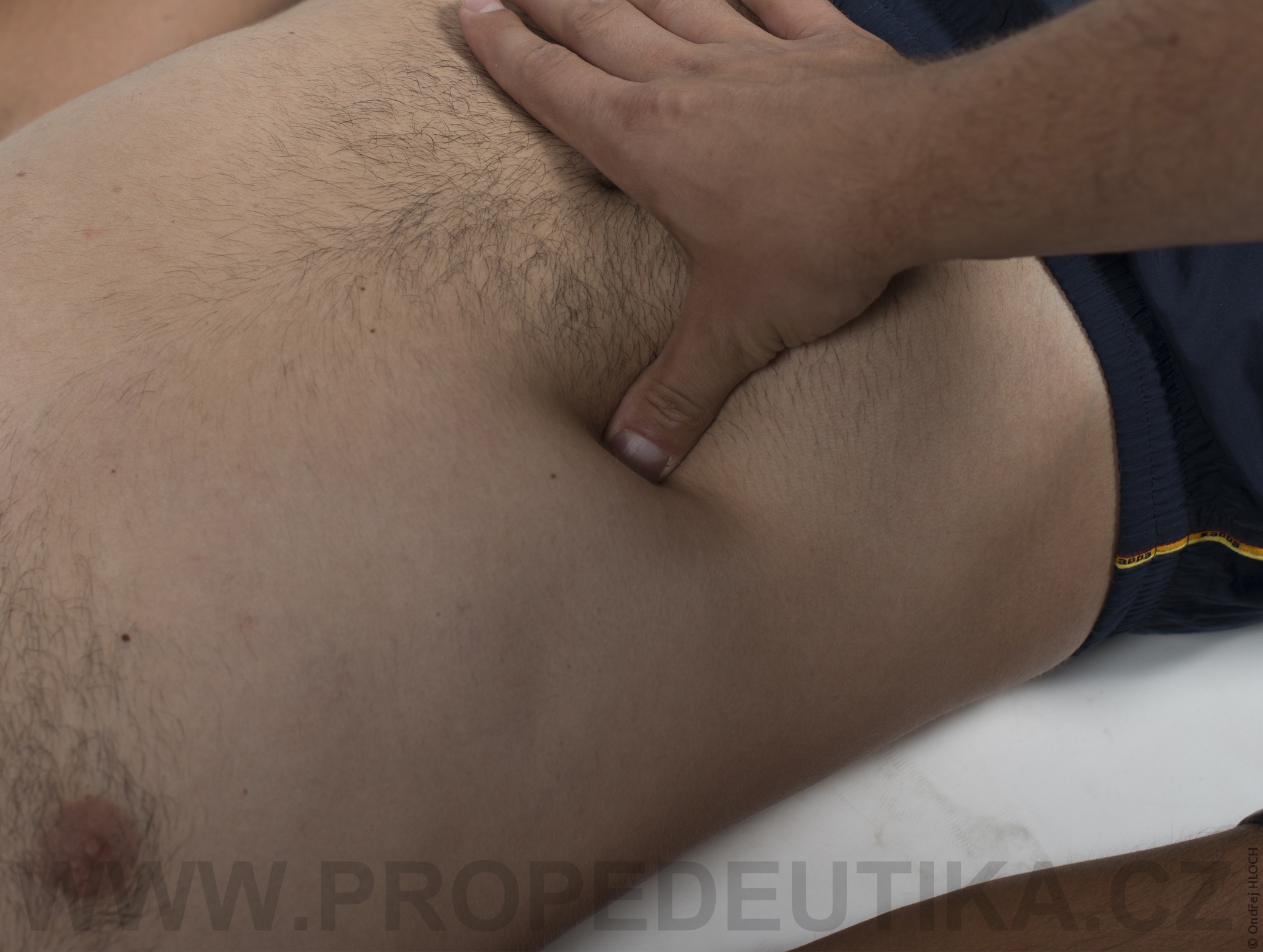
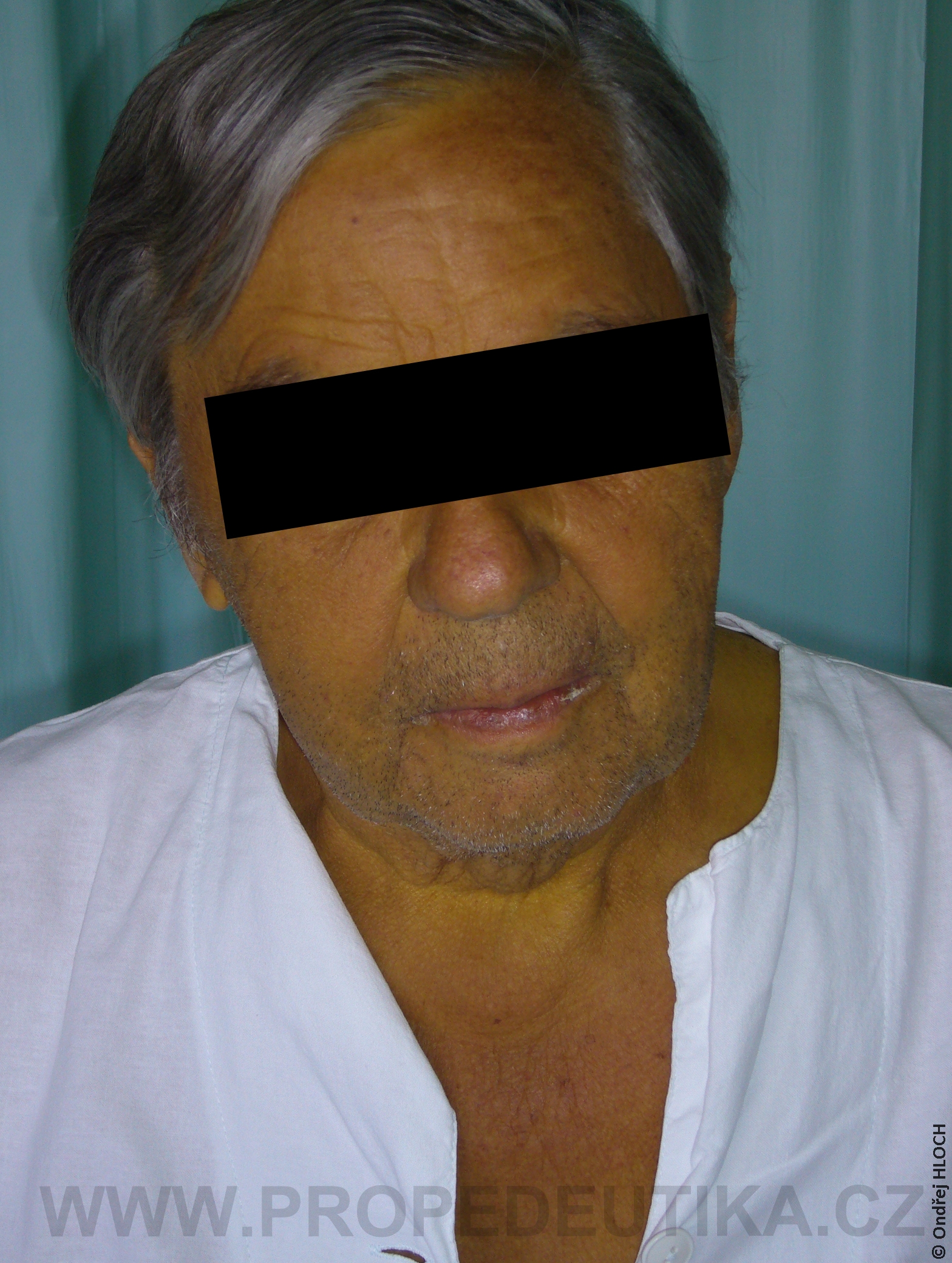
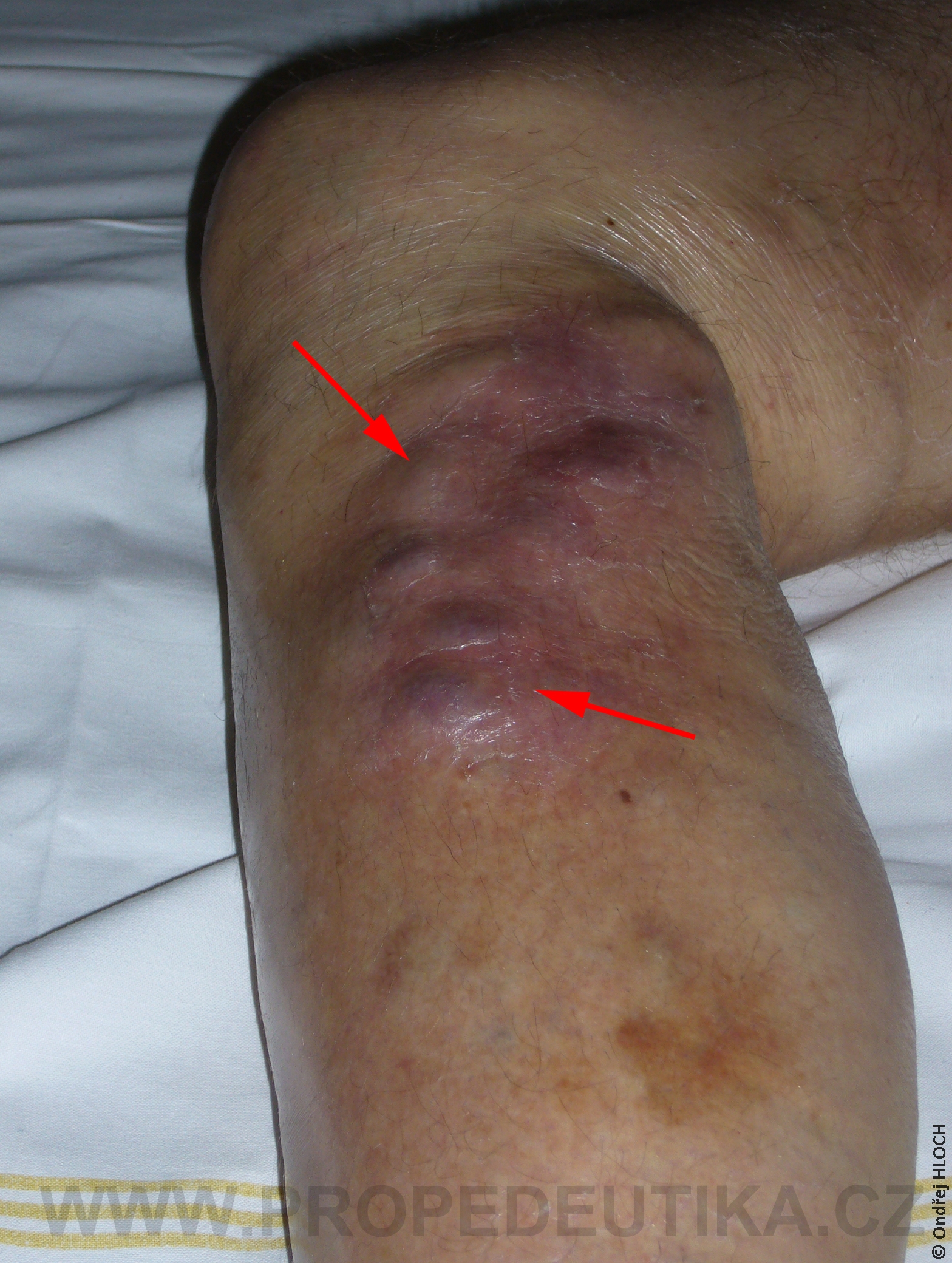
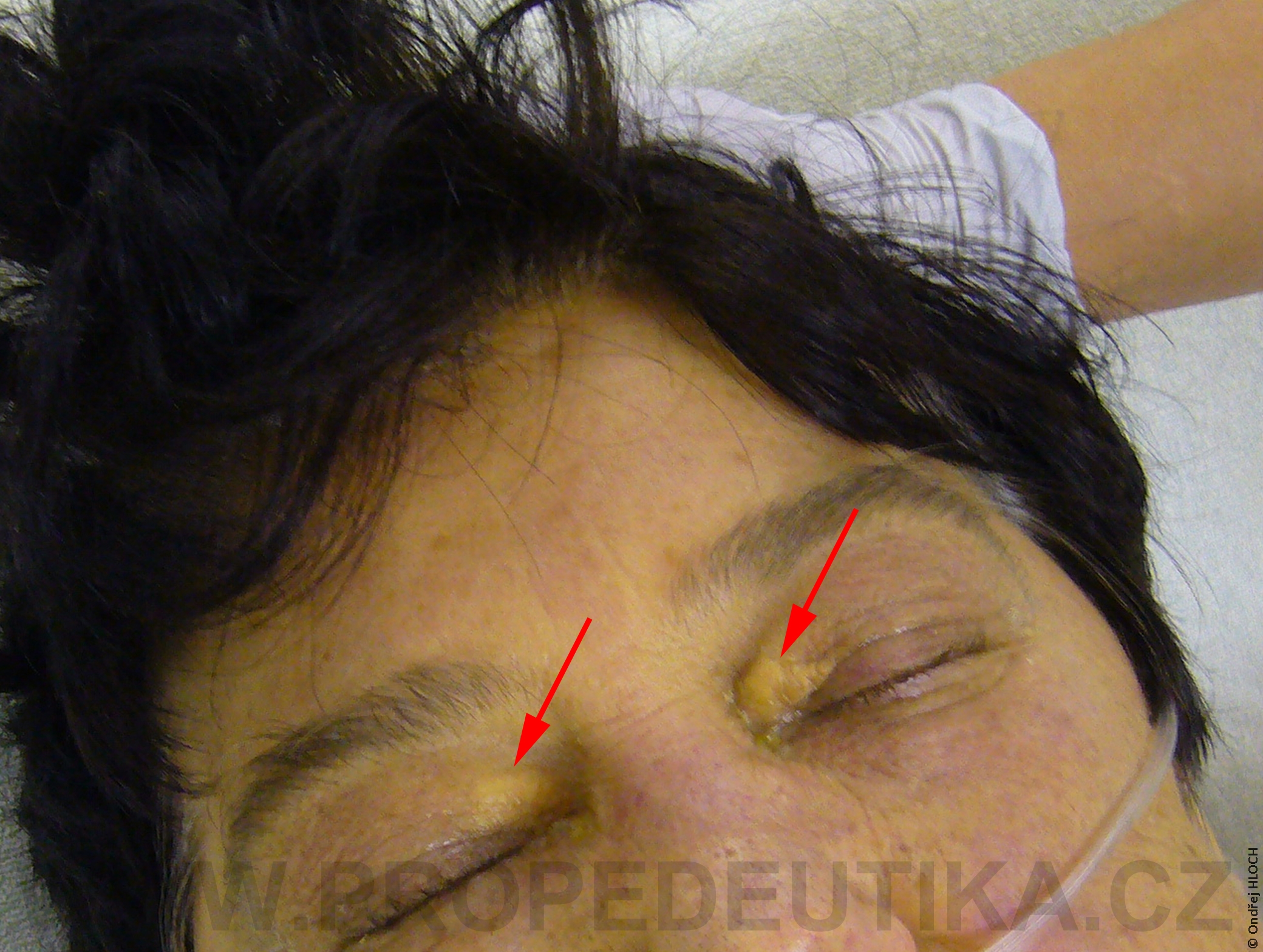
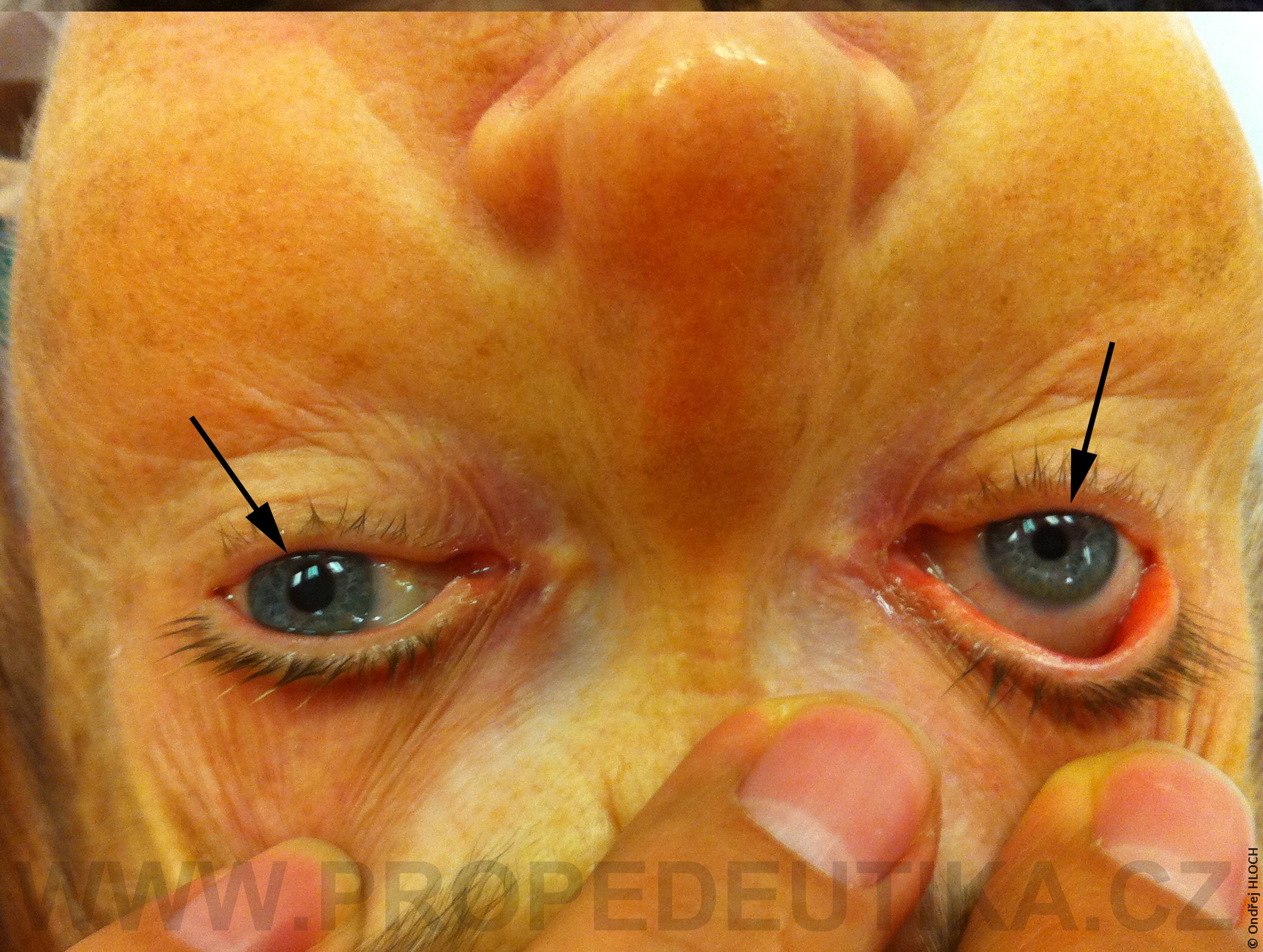
Bilirubin je žlučové barvivo. Vzniká degradací hemoglobinu pocházejícího z rozpadlých červených krvinek. Degradace hemoglobinu se odehrává v buňkách retikuloendotelového systému, což je systém fagocytujících buněk vyskytujících se především v játrech, slezině a lymfatické tkáni. V malém množství vzniká bilirubin i z jiných hemoproteinů (např. z myoglobinu, cytochromů, katalázy). Lidský organismus denně vytvoří asi 300 mg bilirubinu. Vzniklý bilirubin je krví transportován do jater, kde dochází k jeho konjugaci s kyselinou glukuronovou. Konjugace bilirubinu je proces, kterým se bilirubin stává rozpustným ve vodě. Ve vodě rozpustná forma bilirubinu se označuje termínem konjugovaný (přímý) bilirubin. Konjugovaný bilirubin je jakožto součást žluče transportován z jater žlučovými cestami do tenkého střeva. V zažívacím traktu je bilirubin dekonjugován, vzniká tak nekonjugovaný (nepřímý) bilirubin, který je dále degradován (redukován). Nejdůležitějším degradačním produktem bilirubinu je urobilinogen. Laboratorní stanovení koncentrace bilirubinu v krevním séru je důležitým testem, který informuje o rozpadu červených krvinek, funkčním stavu jater a průchodnosti žlučových cest. Současně lze testovat i přítomnost konjugovaného bilirubinu a urobilinogenu v moči. Fyziologická koncentrace celkového bilirubinu (konjugovaného i nekonjugovaného) v krevním séru dospělého jedince činí asi 2,0–17,0 µmol/l.Fyziologická koncentrace konjugovaného bilirubinu v krevním séru dospělého jedince činí 0,0–5,1 µmol/l. Zvýšení bilirubinu v krevním séru nad 17 µmol/l se označuje jako hyperbilirubinémie. Při zvýšení nad 35 µmol/l bilirubin přestupuje z krve do tkání (sliznice, kůže, oční spojivka) a způsobuje jejich žlutavé zbarvení (ikterus).
Testy měřící schopnost a kapacitu jater metabolizovat endogenní a xenogenní látky
Amoniak je v těle tvořen při deaminaci aminokyselin a také činností střevní mikroflóry. Játra jsou vybavena enzymatickými systémy k degradaci amoniaku, který je ve zvýšené koncentraci pro organizmus toxický. Při jaterním onemocnění, a tudíž snížené schopnosti jater eliminovat amoniak, se projevují jeho účinky zejména ve smyslu jaterní encefalopatie.
Vyšetření nespecifických protilátek v diagnostice jaterních onemocnění
Vyšetření jsou prováděna u všech onemocnění, kde předpokládáme podíl autoimunity – především u autoimunitních hepatitid, primární biliární cirhózy, sklerózující cholangoitidy, autoimunitní cholangoitidy. Autoprotilátky jsou však přítomny i u vysokého počtu nemocných s chronickou infekcí HCV. Protilátky jsou druhově nespecifické, mohou se přechodně vyskytnout i u zdravých osob.
Laboratorně je autoimunitní hepatitida charakterizována především elevací aminotransferáz. Zvýšení aminotransferáz je vyšší než vzestup bilirubinu a obstrukčních enzymů, ale vzácně může mít onemocnění i cholestatický charakter. Charakteristická je výrazná hypergamaglobulinémie.
Základní serologické nálezy u autoimunitních hepatitid jsou:
Pozitivita protilátek
- proti buněčným jádrům – ANA
- proti mitochondriím – AMA
- proti jaterním a ledvinných mikrosomům – LKM
- proti hladkému svalu – ASMA
- proti aktinu – AAA
- proti cytoplazmě neutrofilů – pANCA
- proti dvouvláknové DNA – dsDNA
Tkáňová typizace
- pozitivita antigenu B8 a DR 3
- protilátky proti aktinu jsou velmi specifické, ale zatím špatně dostupné, určitou náhradou je vysoký titr protilátek proti hladkému svalu (ASMA).
Imunologická a sérologická diagnostika hepatitid
Hepatitida A
- Prokazujeme anti-HAV protilátkami, provádí se vyšetření specifických protilátek IgM v séru (anti-HAV-IgM), zvýšení transamináz a bilirubinu, mírné zvýšení ALP.
- Negativita testu u imunokompetentních osob nákazu vylučuje.
- IgM přetrvávají v séru 3–6 měsíců po nákaze, IgG přetrvávají dlouhodobě.
Hepatitida B
Antigeny:
- HBsAg (surface, Australský Ag) – 3 podtypy, umožňuje průnik viru do hepatocytu. Jeho průkaz je známkou přítomnosti viru v organismu (v jakémkoli období infekce, u hepatidy akutní i chronické – v replikační i integrační fázi).
- HBcAg (core) – protein obaluje DNA viru, prokazatelný na membráně hepatocytu (imunofluorescence v biopsii), kde je vystaven ve vazbě na MHC II a rozpoznáván TC a NK buňkami, je prokazatelný pouze v období replikace (akutní a chronická replikační fáze).
- HBeAg (secretory) – část HBcAg, která je vylučována pouze během replikace viru (u tzv. wild type virů), jsou možné i mutanty, které HBeAg netvoří, ukazuje na aktivní replikaci viru v jaterní buňce (u akutní a chronické replikační hepatitidy), je známkou vysoké infekciozity nemocného.
Protilátky:
- Anti-HBs – neutralizační (vazbou na HBsAg na povrchu viru brání jeho vstupu do buňky), je v séru osob, které někdy v životě prodělaly HBV infekci (pak bývají přítomny i anti-HBc a anti-HBe), anebo u osob očkovaných (isolovaná anti-HBs positivita).
- Anti-HBc – nejspecifičtější a nejcitlivější protilátka u HBV infekce – je přítomna při jakékoli exposici viru (je stopou, kterou po sobě virus v organismu zanechá).
- Anti-HBe – bývá po prodělané infekci (nikoli v období aktivní replikace viru, kdy převažuje HBeAg).
| HBsAg | anti-HBs | HBeAg | anti-HBe | IgG anti-HBc | IgM anti-HBc | HBV DNA | |
| Akutní VH B | + | – | + | – | + | + | + |
| Chronická VH B-aktivní replikace | + | – | + | – | + | +/– | + |
| Chronická VH B-inaktivní nosičství | + | – | – | + | + | – | – |
| Prodělaná infekce | – | + | – | + | + | – | – |
| Úspěšná vakcinace | – | + | – | – | – | – | – |
V období aktivního zánětu (akutní hepatitida B a chronická hepatitida v replikační fázi) jsou tedy prokazovány HBsAg a HBV DNA (PCR) jako známky přítomnosti viru a dále anti-HBc (s přítomností HBcAg v membráně hepatocytů) a HBeAg.
Při inaktivním nosičství není prokazatelná HBV DNA, v membráně hepatocytů nejsou HBcAg, tudíž se ani neprokazují HBeAg (jsou však protilátky anti-HBc a anti-HBe) – serokonverse HBeAg – anti-HBe.
Po prodělané infekci se prokazují jen protilátky, nikoliv antigeny (serokonverse HBsAg – anti-HBs, HBeAg – anti-HBe)
Hepatitida C
Základním průkazem je sérologicky protilátka anti-HCV (není pouze u infikovaných osob, ale i u těch, které virus eliminovaly spontánně nebo protivirovou léčbou), ukazatelem aktivní infekce je PCR průkaz virové RNA.
Anti-HCV je prokazatelná cca 3 týdny po expozici, nemá preventivní účinek proti reinfekci.
Proto se častěji musíme uchýlit k jaterní biopsii.
Tvorba Ig může být opožděna, při podezření na akutní VHC, je potřeba opakovat.
U chronické hepatitidy C je třeba biopsie se stagingem (pokročilost jaterní fibrózy), který ukáže riziko progrese do jaterní cirhózy.
Virus se nedaří pěstovat na tkáňových kulturách, proto se prokazuje PCR či Ig anti-VHC
Hepatitida D
Provádí se průkaz specifických protilátek proti antigenu delta metodou ELISA
Hepatitida E
- průkazem anti–HEV
- průkaz protilátek IgG a IgM;
Hepatitida G
diagnostika HGV RNA, průkaz anti–HGV svědčí spíše o prodělané infekci, často se kombinuje s VHB nebo VHC
Biochemická vyšetření u vybraných jaterních chorob
Hemochromatóza
- Vysoká saturace transferinu (více než 60% u mužu, 50% u žen), zvýšená koncentrace plazmatického železa, snížená celková vazebná schopnost séra pro železo
- Zvýšená koncentrace ferritinu (norma u mužu do 300Ug/g/l, u žen do 200 pro hemochromatózu svědčí obvykle hodnoty vyšší než 1000
- Potvrzení: jaterní biopsie – průkaz nahromadění železa
- Molekulárně genetické vyšetření – změna na krátkém raménku 6.chromozomu, u 80% postižených mutace C282Y nebo H63D
Wilsonova choroba
- Snížení koncentrace ceruloplazminu pod 0,2 g/l snížení sérové koncentrace mědi, zvýšení frakce volné mědi v séru nad 2,0 Umol/l, zvýšené vylučování mědi močí nad 1,5 Umol/ den
- Potvrzení: zvýšený obsah mědi v jaterní tkáni (pozitivní nález zvýšení nad 250 Ug/g jaterní tkáně
- Molekulárně genetické vyšetření – přímá DNA diagnostika – nejčastější mutace H1069Q
Hepatocelulární karcinom (HCC)
- Zvýšení alfa- fetoproteinu (AFP)
- Zvýšení koncentrace Ca 19-9
- HBV, HCV, hemochromatóza
MUDr. Ladislav DOUDA
ladislav.douda@fnmotol.cz
Použitá literatura:
Zima T.: Laboratorní diagnostika, Galén
Klener et al.: Vnitřní lékařství, 2000
Češka a kolektiv: Interna, Triton
Internet : http://www.wikiskripta.eu/